14%

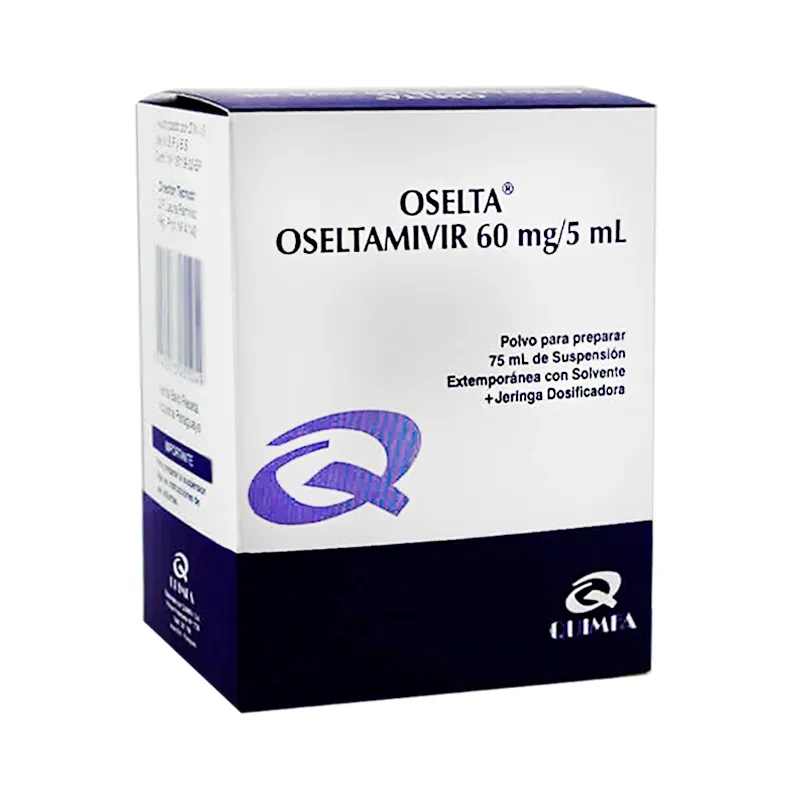
Disemid Oseltamivir 60mg/5ml - Jarabe de 75 mL
Código: 613767840653005020
Retiro de sucursalCalculando
DeliveryCalculando
RegularGs. 181.500
-14% de descuento
Con descuentoPrecio exclusivo para compras vía Web.
Gs. 156.090Descripción
También te podría interesar
También te podría interesar